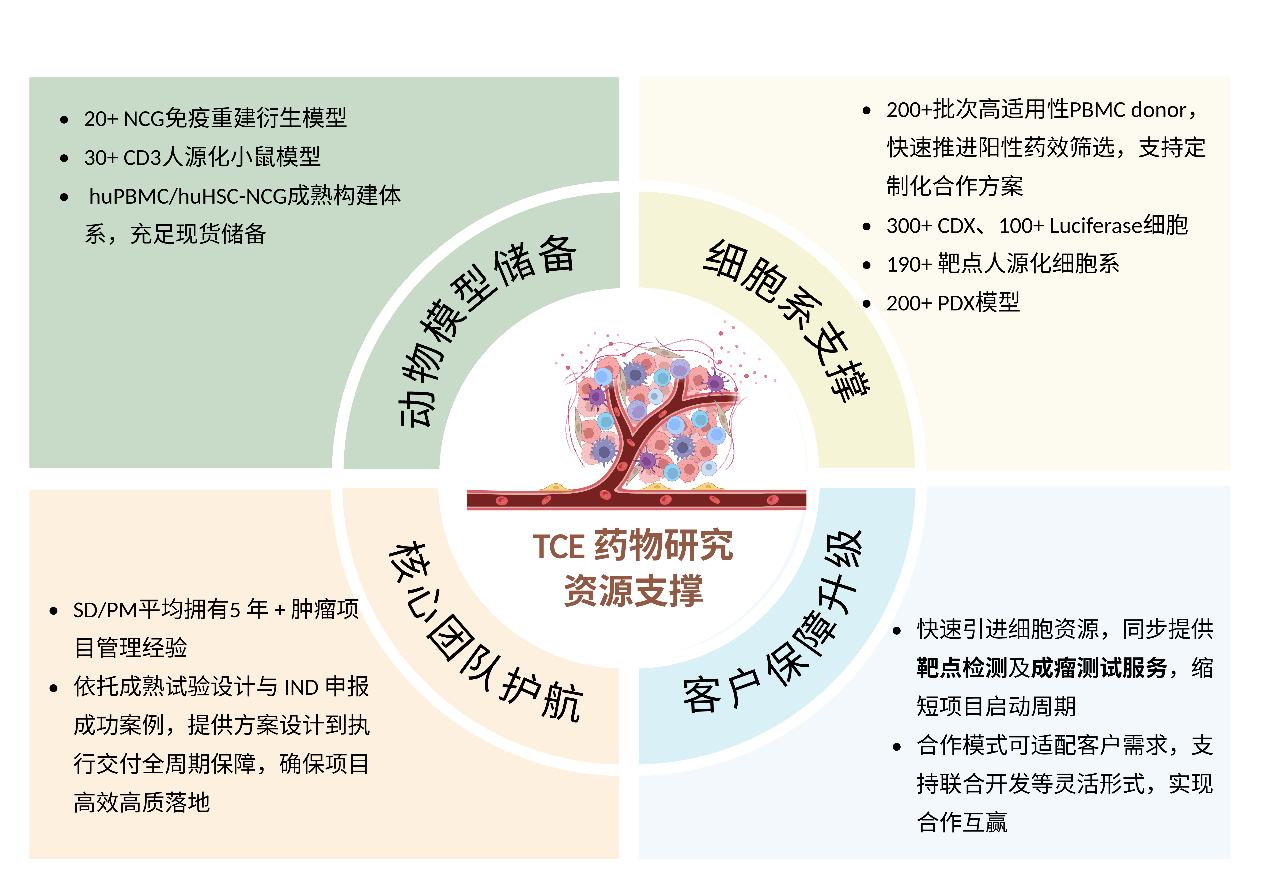
药康生物邀您参加BIOCHINA2026
2026年2月13日 16:02
从血液瘤到实体瘤:TCE技术进展及药康生物一站式临床前解决方案
近年来,肿瘤免疫治疗和细胞治疗在多种肿瘤类型中取得了显著突破,然而在MHC分子下调或免疫浸润不足的实体肿瘤中,疗效往往有限。其中,自体CAR-T疗法虽然展现出强大的杀伤能力,但受限于自体定制周期长、成本高昂以及制备流程复杂等因素。相比之下,TCE(T细胞衔接器)作为标准化的“即用型”蛋白药物,具有开发周期短、生产放大可控、质量一致性高等优势,更有利于推动规模化临床应用。因此,TCE已成为继免疫检查点抑制剂和细胞疗法之后的重要免疫治疗策略。它通过直接桥接T细胞与肿瘤细胞,高效募集并激活内源性T细胞,且不依赖MHC抗原呈递,在免疫抑制性肿瘤微环境中显示出更强的机制优势 (图1)。
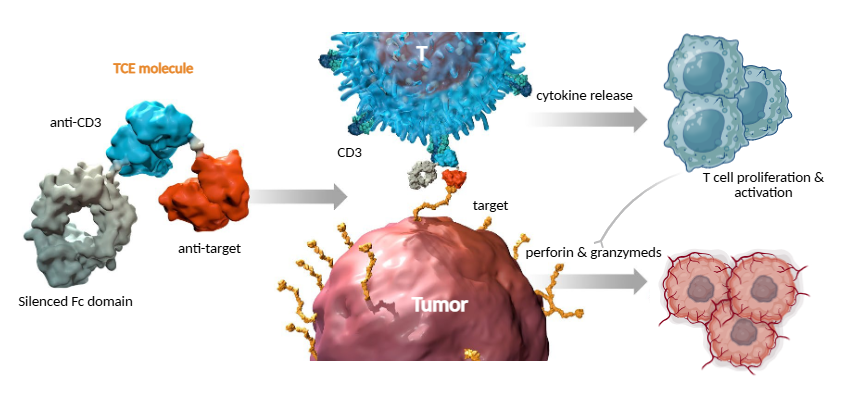
图1. TCE药物作用机制
截至目前,全球已有11款TCE药物获批上市。其中,Tarlatamab-dlle作为首款针对小细胞肺癌(SCLC)的药物,标志着TCE技术从血液肿瘤正式扩展至实体瘤领域,成为该领域的里程碑事件,迅速引发了行业对TCE药物的高度关注。当前,TCE在实体瘤适应症方面已进入临床突破期,SCLC和mCRPC成为进展最快的两大适应症,DLL3、STEAP1、PSMA等靶点成为主流,多项III期研究正在稳步推进。
在TCE向实体瘤规模化应用的过程中,仍面临诸多临床瓶颈需要突破,例如传统TCE存在肿瘤穿透性差、抗原异质性、半衰期短、CRS风险及脱靶毒性等问题。为此,研发热点聚焦于高特异性靶点挖掘、TCR融合拓展胞内抗原、CD3亲和力调控与条件激活设计以降低CRS风险,同时通过半衰期优化、联合免疫/化疗以及mRNA局部递送等方式突破肿瘤微环境限制,旨在平衡疗效与安全性,推动TCE药物的全面发展。
技术创新与临床突破的背后,非临床药效评价是TCE研发中不可或缺的关键环节。TCE在高效介导T细胞杀伤肿瘤的同时,也对临床前药效验证和安全性评估提出了更高要求,包括模型选择、人源化程度、供体差异、药效窗口及药物毒性等。面对这些挑战,药康生物建立了系统化且成熟的TCE药物临床前评价解决方案,以助力TCE药物的非临床药效评价,赋能新药研发。
TCE药物临床前评价
l 体外药物评价
药康生物已建立完善、系统化的TCE体外药效评价体系,围绕靶点结合、T细胞功能及体外杀伤等方面,形成标准化且经验丰富的评价流程。
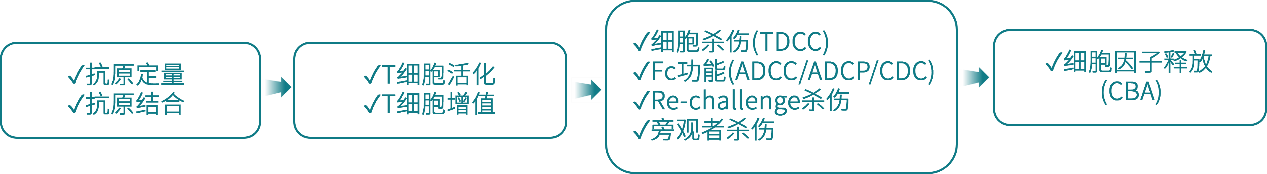
l 体内药效评价
药康生物基于自主研发的NCG及NCG-MHC-dKO模型,建立了多种适应症的PBMC荷瘤药效评价体系,并储备了200多批次高适用性PBMC供体,可快速推进项目进展。此外,通过定期构建HSC重建模型,建立了基于HSC的TCE药物评价体系,满足长周期药物评价及non-GLP安全性评价需求。同时,药康生物拥有双背景hCD3人源化小鼠,并适配190多个靶点的人源化改造鼠源细胞,积累了丰富的TCE药效数据及机制研究经验;平台还构建了30多种CD3与TAA双人源化小鼠,支持TCE安全性评价研究。
图2. 根据待测药物MOA及肿瘤特性选择最优方案
案例分享
Xaluritamig(CD3-STEAP1)体内外的药效评价
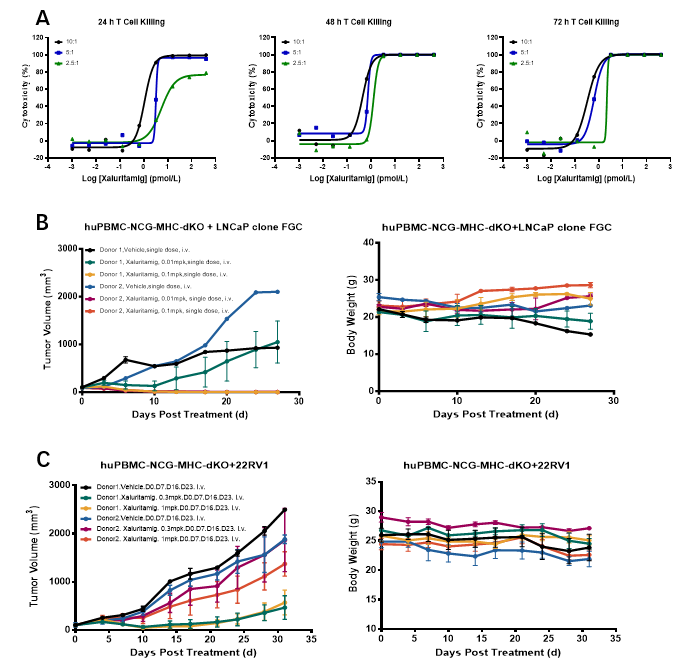
图3. Xaluritamig体外及体内药效评价
A:Xaluritamig在体外可有效发挥TDCC作用;B: Xaluritamig在体内对LNCaP clone FGC(STEAP1 高表达细胞系)有显著肿瘤生长抑制作用;C: Xaluritamig在体内对22RV1(STEAP1低表达细胞系)有显著肿瘤生长抑制作用。
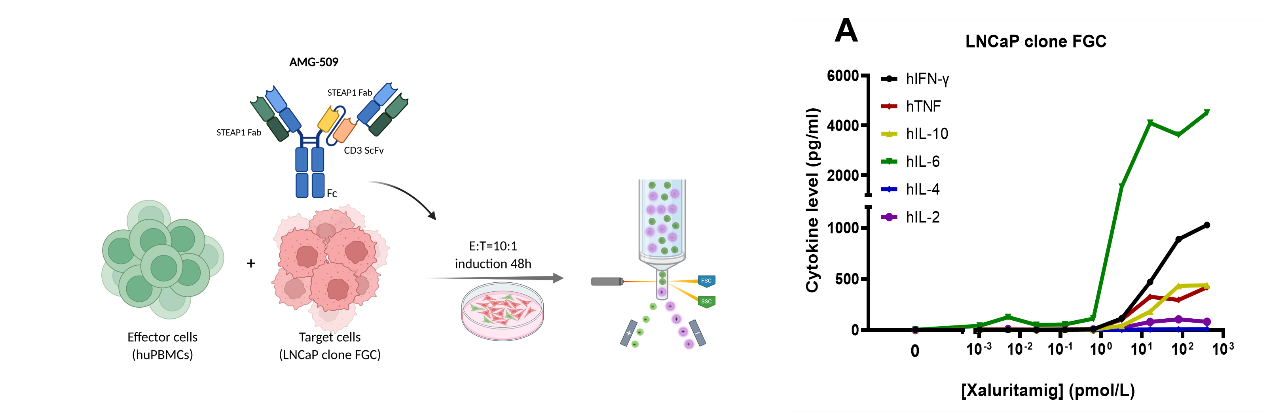
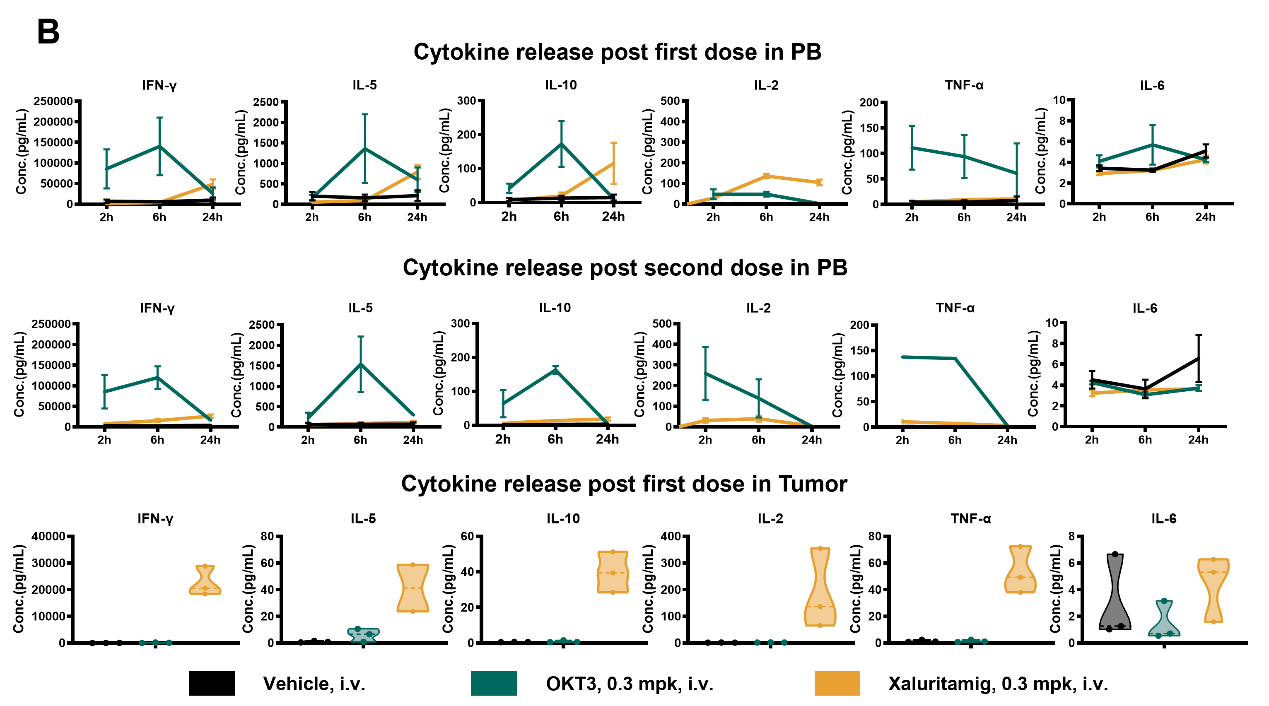
图4. 体外及体内Xaluritamig 诱导的细胞因子释放
A: Xaluritamig可有效激活抗肿瘤免疫应答;B: 药物可在肿瘤局部可有效激活免疫应答,且引发细胞因子释放综合征(CRS)的风险较低。
TCE 药物能将 T 细胞精准靶向至肿瘤细胞并强效激活,杀伤效率高、给药便捷、研发与生产成本相对更低,临床转化潜力突出,在血液肿瘤与实体瘤中均有广阔应用前景。
药康生物提供从体外评价到体内药理药效、非临床(non-GLP)毒理研究的全链条整合服务,覆盖TCE药物研发关键环节,为研究TCE药物的有效性,安全性提供了系统、可靠且高效的非临床评价载体,赋能TCE药物临床前药效验证,为药物筛选、机制验证与风险评估提供高质量全方位支持。